来源:国家药品监督管理局 7月21日,国家药监局发布关于25批次药品不符合规定的通告(2020年 第50号),经河南省食品药品检验所等9家药品检验机构检验,14家药品生产企业生产的25批次药品不符合规定。不符合规定项目分别为溶液的澄清度与颜色、装量、溶出度、可见异物、粒度、含量测定、检出金胺O、性状等。 目前,药品监督管理部门已要求相关企业和单位采取暂停销售使用、召回等风险控制措施,对不符合规定原因开展调查并切实进行整改。
国家药监局关于25批次药品不符合规定的通告(2020年 第50号)
经河南省食品药品检验所等9家药品检验机构检验,标示为江苏吴中医药集团有限公司苏州制药厂等14家药品生产企业生产的25批次药品不符合规定。现将相关情况通告如下: 一、经河南省食品药品检验所检验,标示为江苏吴中医药集团有限公司苏州制药厂生产的9批次注射用硫酸阿米卡星不符合规定,不符合规定项目为溶液的澄清度与颜色。 经广西壮族自治区食品药品检验所检验,标示为安徽国正药业股份有限公司生产的1批次复方愈创木酚磺酸钾口服溶液不符合规定,不符合规定项目为装量。 经江苏省食品药品监督检验研究院检验,标示为湖南华纳大药厂股份有限公司生产的1批次兰索拉唑肠溶片不符合规定,不符合规定项目为溶出度。 经上海市食品药品检验所检验,标示为海南通用康力制药有限公司生产的4批次注射用奥扎格雷钠不符合规定,不符合规定项目为可见异物。 经湖北省药品监督检验研究院检验,标示为长春人民药业集团有限公司生产的1批次婴儿健脾散不符合规定,不符合规定项目为粒度。 经四川省食品药品检验检测院检验,标示为江西鸿烁制药有限责任公司生产的1批次元胡止痛片不符合规定,不符合规定项目为含量测定;标示为天津同仁堂集团股份有限公司、广东省惠州市中药厂有限公司生产的2批次元胡止痛片检出金胺O。 经中国食品药品检定研究院检验,标示为河北济鑫堂药业有限公司生产的1批次广藿香不符合规定,不符合规定项目为性状。 经安徽省食品药品检验研究院检验,标示为重庆三立堂中药制药有限公司、成都吉安康药业有限公司、内江良辉药业有限公司生产的3批次黄精不符合规定,不符合规定项目为性状。 经大连市药品检验检测院检验,标示为新疆本草堂药业有限公司生产的1批次前胡不符合规定,不符合规定项目为性状。 经中国食品药品检定研究院检验,标示为成都市祺隆中药饮片有限公司生产的1批次制川乌不符合规定,不符合规定项目为性状。 二、对上述不符合规定药品,药品监督管理部门已要求相关企业和单位采取暂停销售使用、召回等风险控制措施,对不符合规定原因开展调查并切实进行整改。 三、国家药品监督管理局要求相关省级药品监督管理部门依据《中华人民共和国药品管理法》,组织对上述企业和单位生产销售假劣药品的违法行为立案调查,并按规定公开查处结果。 特此通告。
国家药监局 2020年7月21日
—— 01 —— 25批次不符合规定药品名单 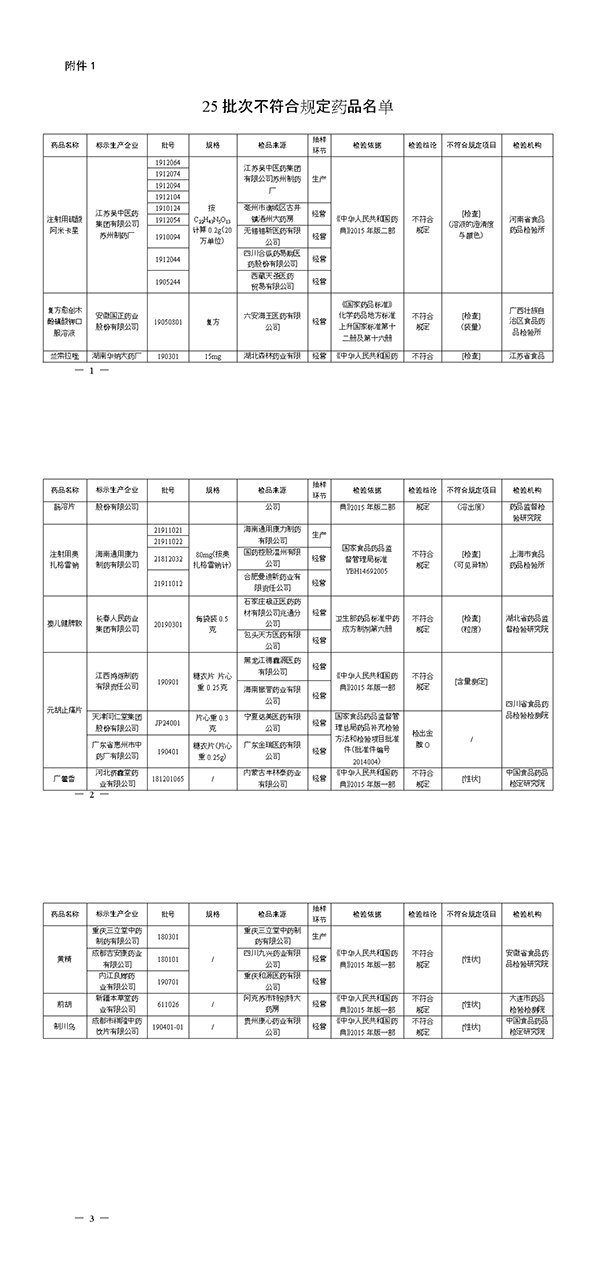
—— 02 —— 不符合药物规定项目的小知识 1. 溶液的澄清度是将药品溶液与规定的浊度标准液相比较,用以检查溶液的澄清程度;溶液的颜色是将药物溶液的颜色与规定的标准比色液比较,或在规定的波长处测定其吸光度。溶液的澄清度与颜色可以在一定程度上反映药物的纯度,是一种能够快速、简便、准确进行药品质量检查的方法。
2. 装量系反映药品重量或容量的指标,适用于固体、半固体、液体制剂,规定应按最低装量检查法进行检查,不符合规定会导致临床给药剂量不足。
3. 溶出度系指活性药物从制剂中溶出的速率和程度,不符合规定会影响药物的吸收,降低生物利用度。
4. 可见异物系指存在于注射剂、眼用液体制剂中,在规定的目视条件下能够观察到的不溶性物质,其粒径或长度通常大于50微米。
5. 粒度系指颗粒的大小,药品中对有粒度要求的制剂产品如颗粒剂、散剂、混悬型滴眼液、混悬型软膏剂等会进行该项目的设定,不符合规定可能会导致药物主成分含量不均一。
6. 含量测定项系指用规定的试验方法测定原料及制剂中有效成分的含量,一般可采用化学、仪器或生物测定方法。
7. 金胺O是一种色素或者染料,检出该成分,提示有染色现象。 8. 性状项下记载外观、臭、味、溶解度以及物理常数等,在一定程度上反映药品的质量特性。中药饮片性状项不符合规定,可能涉及药材种属偏差、炮制工艺有瑕疵、储存不当等情形。 如涉及知识产权请与我司联系
|