未来5年最畅销的抗肿瘤药物TOP10 (亿美元) |
|
2020-03-30 |
访问次数:4346 |
|
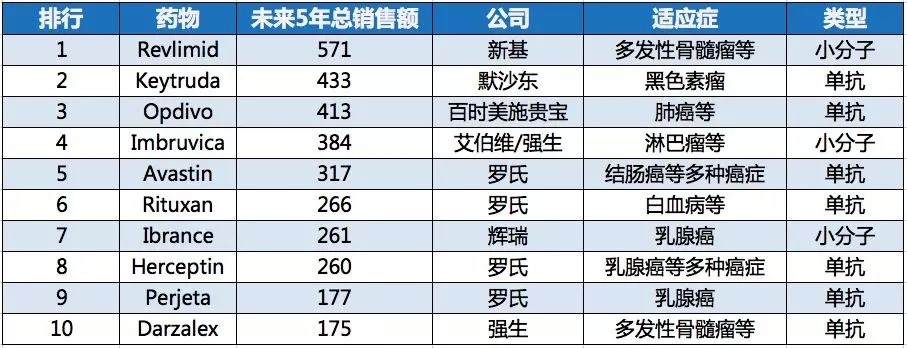
TOP10 Darzalex 达雷木单抗
Darzalex(Daratumumab,达雷木单抗)是一种靶向于CD38的单克隆抗体,2015年成为首个被批准治疗多发性骨髓瘤(MM)的单抗药物。它通过结合肿瘤细胞跨膜胞外酶CD38分子,触发多种免疫机制诱导肿瘤细胞的快速死亡。同时,也有研究证明Darzalex能够靶向肿瘤微环境中的免疫抑制细胞,从而表现出免疫调节活性。
2015年11月首次获批时,Darzalex是作为四线治疗药物使用;2016年11月,该药的2种三联方案(联合来那度胺和地塞米松,联合硼替佐米和地塞米松)获FDA批准,用于既往接受过至少一种疗法的MM患者(二线治疗);2017年6月,Darzalex的另一种三联方案(联合泊马度胺和地塞米松)获FDA批准,用于既往接受过至少2种疗法的MM患者(三线治疗);2017年11月强生又向FDA提交了Darzalex联合硼替佐米、马法兰及泼尼松,用于不适合自体干细胞移植(ASCT)的新诊多发性骨髓瘤(MM)患者的治疗,若获批将成为首个一线治疗的适应症。此外,Darzalex的潜在适应症还包括多种白血病和淋巴瘤,强生还在进行该药的各种适应症临床研究。
Darzalex在上市的第二个年头销售额已经高达12.42亿美元,预测2022年将达到50亿美元,未来5年总销售额175亿美元。
TOP9
Perjeta 帕妥珠单抗
Perjeta(Pertuzumab,帕妥珠单抗)是一种靶向于人表皮生长因子受体2(HER2)的单克隆抗体,通过结合HER2,阻滞HER2与其它HER受体的杂二聚,从而减缓了肿瘤的生长。
Perjeta在2012年6月被FDA批准与赫赛汀和紫杉醇联合使用,用于HER2阳性并且没有接受过抗HER2治疗或化疗的转移性乳腺癌患者;2017年12月,FDA批准基于Perjeta的三联疗法,作为HER2阳性、有高复发风险的早期乳腺癌患者的术后辅助疗法,患者需要接受基于Perjeta的辅助治疗方案一年;FDA还将之前颁布给这款基于Perjeta的治疗方案的(术前)新辅助疗法从加速批准状态改为完全批准,用于HER2阳性患者;2018年1月,Perjeta在中国的上市申请获得CFDA药品审评中心(CDE)受理,预计年内能在中国上市。
Perjeta2017年销售额为23.6亿美元,同比增长26.5%,预测2022年销售额40亿美元,未来5年总销售额177亿美元。
TOP8 Herceptin 赫赛汀
Herceptin是靶向于HER2的人源化单克隆抗体,有15%-20%的乳腺癌病人癌细胞HER2是过表达的,这导致了癌细胞生长的失控。
Herceptin早在1998年就被FDA批准上市,是最早上市的靶向治疗药物之一,目前已经是治疗HER2阳性弥散性乳腺癌的黄金标准,市场占有率高达90%以上,最近几年的年销售额一直维持在60亿美元以上。市场上已经开始有其仿制药物出现:2017年7月安进和梯瓦旗下两种Herceptin仿制药的审批文件被FDA接受, Mylan和Biocon的Herceptin生物类似药也获得FDA推荐审批。2017年11月,罗氏向法院提起诉讼,状告辉瑞公司开发的生物类似药PF-05280014侵犯了Herceptin设计的40多项专利。罗氏要求如果辉瑞公司在Herceptin相关专利失效前上市,辉瑞应向基因泰克支付补偿费用。
罗氏的强硬态度延缓了Herceptin仿制药的冲击,该药2017年销售额高达75.3亿美元,同比增长9.1%。不过,Herceptin的专利到期只是时间问题,届时销售额将大幅下滑,预测2022年销售额45亿美元,未来5年总销售额260亿美元。
TOP7
Ibrance 帕博西尼
Ibrance是一种口服性CDK抑制剂,它是全球首个被批准上市的CDK4/6抑制剂。CDK4/6(细胞周期蛋白依赖性激酶4和6)是调节细胞周期的关键因子,能够触发细胞周期从生长期(G1期)向DNA复制期(S1期)转变,CDK4/6 抑制剂将细胞周期阻滞于G1 期,从而起到抑制肿瘤增殖的作用。Ibrance对CDK4和CDK6 的抑制活性的 IC50 值分别为 11 nM和16 nM。
2015 年 2 月,FDA批准Ibrance用于一线治疗 ER+/HER2-绝经后晚期乳腺癌;2016年4月,FDA批准Ibrance用于二线治疗治疗ER+/HER2- 绝经后晚期乳腺癌。2017年3月Ibrance被批准用于联合芳香化酶抑制剂(之前为联合来曲唑)作为内分泌治疗为基础的初始方案用于治疗HR+/HER2- 绝经后晚期或转移性乳腺癌。不过,Ibrance在英国却遭遇滑铁卢,2017年2月英国国家卫生与临床优化研究所(NICE)表示,Ibrance治疗成本太高不具有成本效益,不推荐将该药用于雌激素受体阳性(HR+)、人类表皮生长因子受体2阴性(HER2-)局部晚期或转移性乳腺癌患者的治疗。但这并没有阻挡其销售额增长的脚步,2017年销售额达到31.3亿美元,同比增长46%。
全球医药行业调研机构GlobalData发布报告指出 Ibrance将主导HR+乳腺癌,预测2022年销售额将超过60亿美元,未来5年总销售额261亿美元。
TOP6 Rituxan 美罗华
Rituxan是一种抗CD20单克隆抗体,1997年被批准上市,是最早的靶向单抗药物。该药是少有的跨越肿瘤(非霍奇金淋巴瘤、慢性淋巴细胞白血病等)和自身免疫疾病(类风湿性关节炎、血管炎等)这两大适应症的药物,Rituxan的销售额大部分来自肿瘤领域,近几年销售额在55亿美元以上。不过,鉴于目前市场已经趋于成熟,该药增长空间有限。
为继续发掘销售增长潜力,罗氏在2016年推出了一款皮下注射的剂型,可以减少注射次数,更适合病人用药。事实证明这一决策十分明智,Rituxan的2017年销售额高达79.35亿美元,同比增长9.8%,这对于一个上市超过20年,面临众多仿制药竞争的药物来说几乎是个奇迹。不过也有业内人士称这是Rituxan的销售峰值了,截止2017年底,该药在欧洲、印度、拉美多个国家都有仿制药物上市。2019年美国专利到期,届时Rituxan的销售将大幅度下滑,预测2022年销售额40亿美元,未来5年总销售额266亿美元。
Top5 Avastin 阿瓦斯汀
Avastin是一种重组的人类单克隆IgG抗体,通过抑制人血管内皮生长因子的生物学活性而起作用。
由于血管生成异常现象在实体瘤中非常普遍,因此Avastin的适应症非常广泛,自从2004年首次被批准用于治疗结直肠癌之后,该药适应症已经扩大至最常见的肺癌、乳腺癌等;而罗氏至今还没有停止研究开发其新的适应症,在2017年罗氏还提交了一个用于治疗间皮瘤的申请,同时还有与罗氏的新药Tecentriq联合用药的临床研究。虽然相对于Herceptin和Rituxan,Avastin面对的生物仿制药竞争相对较小,但对于未来销售额也有着一定影响。目前,Avastin已经有一些仿制药在印度、俄罗斯等监管不严的新兴市场上市,还有多个公司的仿制药物虎视眈眈中,如安进 / 艾尔建的 ABP 215、辉瑞的PF-06439535,这二者都已经完成了临床研究,此外像三星旗下Bioepis、勃林格殷格翰、AryoGen等制药公司的仿制药都已到III期临床的阶段。
Avastin的2017年销售额为71.4亿美元,同比增长了4.6%,预计2022年销售额47亿美元,未来5年总销售额317亿美元。
TOP4 Imbruvica 依鲁替尼
Imbruvica是首个上市的Bruton'styrosine kinase (BTK)抑制剂。BTK 是 BCR 通道可识别的信号肽分子,当该信号肽分子穿过 B 淋巴细胞表面受体时, B 淋巴细胞实现转运、趋化性和黏附作用的必需通道被激活,这为 B 细胞恶性肿瘤的形成提供了便利。Imbruvica是一种小分子的 BTK 抑制剂,可与BTK 活性位点上的半胱氨酸残基( Cys-481)选择性地共价结合,不可逆地抑制 BTK 的活性。
目前,Imbruvica获批的适应症有套细胞淋巴瘤、慢性淋巴细胞白血病、华氏巨球蛋白血症等7个。2018年2月,FDA授予Imbruvica治疗胃癌(包括胃食管连接腺癌)的孤儿药资格,并且该药治疗胰腺癌的Ⅲ期临床研究也已经进行中。Imbruvica已于2017年8月获中国CFDA批准上市,单药用于既往至少接受过一种治疗的慢性淋巴细胞白血病/小淋巴细胞淋巴瘤患者以及既往至少接受过一种治疗的套细胞淋巴瘤患者的治疗。
Imbruvica的销售表现非常强势,可以和PD-1单抗Opdivo媲美,2017年销售额44.7亿美元,同比增长44.9%,增长幅度远超Opdivo(31.1%)。预测2022年销售额90亿美元,未来5年总销售额384亿美元。
TOP3 Opdivo 纳武单抗
Opdivo(Nivolumab)几乎就是PD-1单抗的代名词,其发展就是近年来肿瘤免疫药物蓬勃发展的一个缩影。
Opdivo是全球首个被批准的PD-1单抗,2014年以来,该药被批准的上市适应症已经多达8个,包括非小细胞肺癌、经典型霍奇金淋巴瘤、肝癌、结直肠癌、黑色素瘤等常见的肿瘤。与此同时,BMS还在进行多项临床研究,其适应症将不断扩大。最近有报道称Opdivo甚至能用于HIV治疗领域:用Opdivo治疗感染了HIV的肺癌患者时,观察到能够躲避抗逆转录病毒疗法攻击的HIV细胞储存“剧烈和持续下降”。当然,这只是其中的一个临床现象,距离上市治疗HIV感染还有相当遥远的距离,Opdvio的主战场还是抗肿瘤领域。
目前Opdivo的销售额比同样是免疫治疗领域的明星药物Keytruda要略胜一筹,但其增长势头明显弱于Keyturda。为保持其领先地位,目前有多个临床项目正在进行中,2018年2月,BMS宣布Opdivo+Yervoy在一线治疗伴有较高肿瘤突变负荷(TBM)的NSCLC患者(不考虑PD-L1表达水平)的关键III期CheckMate-227中到达主要终点,相比化疗可以显著延长PFS。Opdivo+Yervoy成为首个取得生存获益的免疫药物组合。CheckMate-227研究将会继续进行,以评估Opdivo+Yervoy能否到达改善OS的主要终点。
该药2017年销售额为49.4亿美元,预测2022年销售额100亿美元,未来5年总销售额413亿美元。
TOP2 Keytruda 派姆单抗
Keytruda(Pembrolizumab)是首个被FDA批准上市的PD-1单抗,它和BMS的Opdivo在PD-1抑制剂的市场可谓绝代双骄。
Opdivo从2015年以来销售额一直遥遥领先Keytruda,2017年度Opdivo销售额为49.4亿美元,远超Keytruda的38.1亿美元销售额。但是二者的差距正在逐渐缩小,2017年Q4两者销售额几乎已经持平:13.6亿美元对13.0亿美元。并且,随着Keytruda临床研究推进,累计被批准的适应症已经达到了9个,包括黑色素瘤、非小细胞肺癌、头颈部癌、霍奇金淋巴瘤、胃癌等常见的肿瘤,此外Keytruda还适用于所有带MSI或dMMR的实体肿瘤患者;2018年1月默沙东公司公布了Keytruda临床试验KEYNOTE-224的最新临床数据,此项临床II期试验旨在评价Keytruda在Sorafenib经治的晚期肝细胞癌患者中的安全性和有效性。这些好消息的到来,让业界对keytruda的前景也较为看好,未来该药极有可能在与Opdivo的竞争中实 现逆袭,二者的胜负可能就在几个临床研究的成败中分出。
预测Keytruda的2022年销售额110亿美元,未来5年总销售额433亿美元。
TOP1 Revlimid 来那度胺
Revlimid最初获批用于多发性骨髓瘤的二线治疗,目前已经广泛应用于多发性骨髓瘤的一线治疗,同时其他适应症范围不断扩大,包括骨髓增生异常综合症,复发或者难治的套细胞淋巴瘤,至少接受过两次治疗的套细胞淋巴瘤,弥散性大B细胞淋巴瘤,造血干细胞移植后多发性骨髓瘤患者的维持治疗等。
Revlimid的开发历程颇为传奇:该药是由臭名昭著Thalidomide(沙利度胺,反应停)改造而来的。Thalidomide曾经引发了数万畸形儿的产生,但是上世纪末人们发现其在抗炎、抗血管生成等方面有奇效,经过进一步的药物改造和临床研究,就催生了如今这款重磅药物。在生物药大行其道的今天,Revlimid作为一种小分子药物还能在最畅销榜上处于前列,说明其功效还是值得肯定的。
Revlimid在未来几年内都不会受到仿制药竞争的问题,其欧洲专利2024年到期,而美国市场更是到2027年专利才到期。因此该药销售额未来将继续不断上升,2017年销售额81.87亿美元,预计2022年销售额将超过130亿美元,未来5年总销售额571亿美元。
返回最上面
|
|