▉ 前言 上一期推送中我们为大家介绍了免疫恢复过程中,iTreg细胞和TGF-β细胞因子的作用,它们作为免疫反应的“镇静剂”,在威胁得到控制的时候,避免免疫反应进一步增强(物极必反)。本期推送中,我们将进一步学习免疫恢复过程T细胞经历的变化及其作用机制。 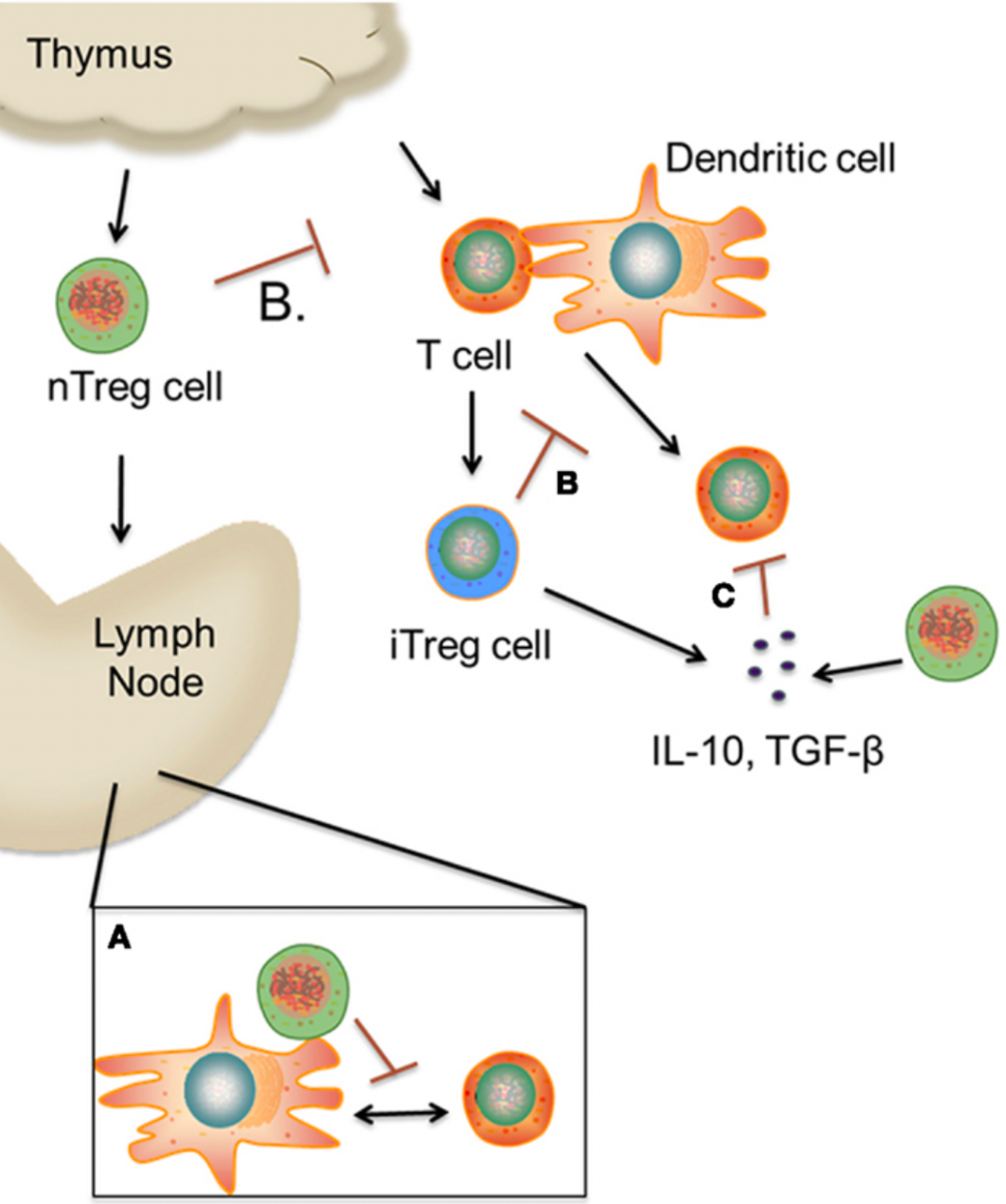
随着威胁的解除,APC提呈抗原数量降低,固有免疫带动适应性免疫水平降低,免疫反应得到控制。然而,仅仅控制源头还不行,因为T细胞还处于活化状态,面对“投降”的敌兵,如果“T将军”率领的部队还保持高昂的斗志,很容易对机体造成损伤。因此,我们接下来要做的工作是“稳住T”。 ▉CTLA-4和PD-1\PD-L1 免疫激活过程中,初始T细胞在TCR与APC的MHC-肽识别后,通过T细胞CD28分子与APC表面B7分子结合,实现T细胞活化。然而B7分子对CD28并非“情有独钟”,它也可以和CTLA-4结合,而且其亲和强度是CD28的数千倍。那么,CTLA-4何许人也?
CTLA-4同CD28,均为免疫球蛋白相关受体家族成员,负责T细胞免疫调节的各方面。在大多数T细胞表达CD28的同时,CTLA-4在初始T细胞中孕育,存储于细胞内。距离本轮T细胞活化约两天后,CTLA-4开始由初始T细胞内部转移到细胞表面,抢占几乎所有的APC B7位点。自此,CD28“形单影只”。CTLA-4不会使初始T细胞活化,适应性免疫逐渐关闭。“T部队后备力量”被扼杀,那么“T部队老将”呢? 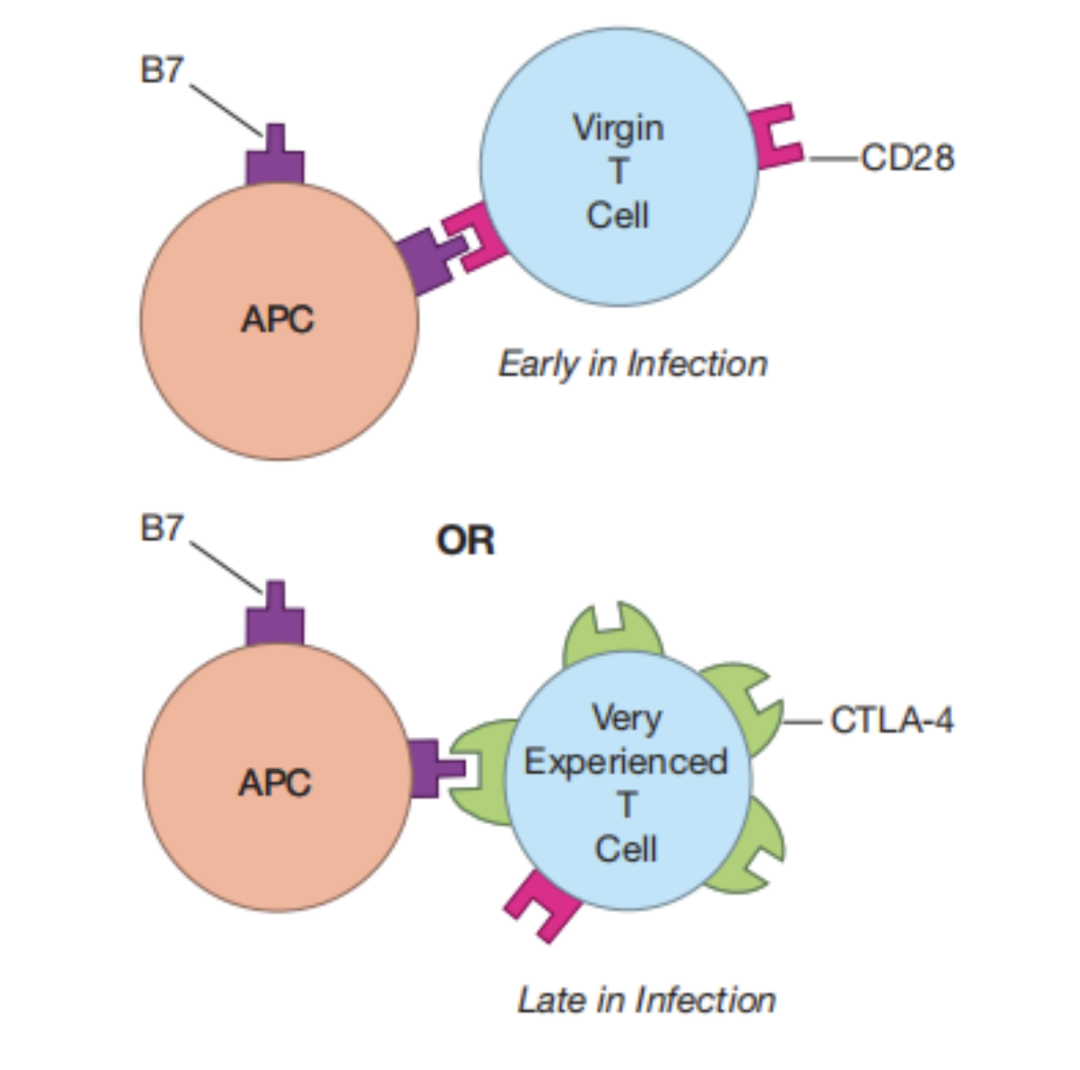
随着“T部队老将”驰骋沙场,在细胞表面逐渐赋予PD-1标志。作为PD-1的搭档,PD-L1在多种炎性组织中表达。当PD-1和PD-L1结合,“T部队老将”就像喝醉了一样,不能继续执行任务。(如此设计,可以避免混乱,即不会牵连其他刚打响的战役,在那个战场上,那里的将军依然是英姿飒爽,奋勇杀敌。)
生物学上,CTLA-4和PD-1被称作“免疫检查点”,发挥负免疫调节作用。 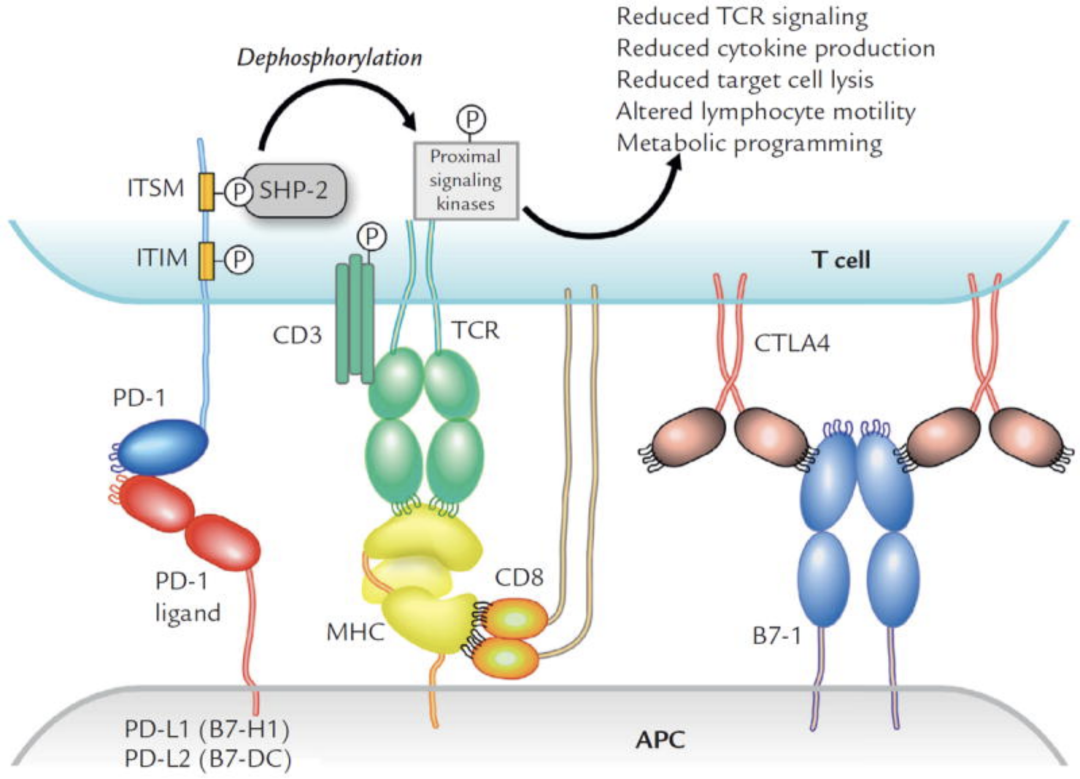
来源:《The Next Immune-Checkpoint Inhibitors: PD-1/PD-L1 Blockade in Melanoma》 肿瘤微环境(TME)内,肿瘤细胞和APC上,PD-L1的高异常表达,介导了肿瘤逃逸。近几年,PD-1/PD-L1通路因其显著的临床效果、持久反应性和低毒力得到众多科学家的热捧。癌症治疗中,靶向PD-1/PD-L1通路目的不是增强免疫系统对肿瘤的反应性,而是让免疫系统保持正常活性,解除PD-1/PD-L1通路对其抑制。该方法也并非万能,只对部分病人有效。 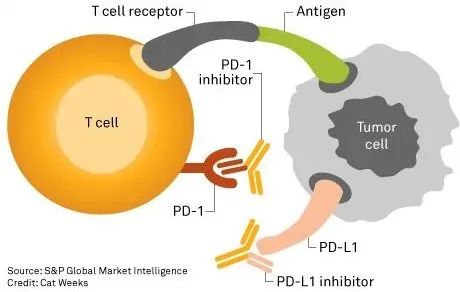
肿瘤浸润淋巴细胞(TIL)上多有PD-1表达。对于CD4+TIL,Treg细胞一般PD-1表达增加,这些活化的Treg细胞预示着TME处于免疫抑制状态。对于CD8+TIL,PD-1表达增加将导致其处于无能或耗竭状态,即失去CTL功能。
同样,肿瘤相关巨噬细胞(TAMs)表达PD-1,导致其对肿瘤细胞吞噬能力降低。在实体瘤和血液瘤,肿瘤细胞PD-L1表达上调。
▉ 总结 PD-1/PD-L1通路在自身免疫病、病毒感染、移植免疫和肿瘤免疫中具有重要作用。 正常情况下,PD-1/PD-L1通路诱导、维护外周免疫耐受,对防止组织产生过度炎症和自体免疫疾病具有积极意义。然而,在肿瘤发生发展过程中,PD-1/PD-L1通路抑制宿主抗肿瘤反应,导致肿瘤免疫逃逸,具体机制如下: 1、抑制TIL活化并诱导其凋亡 2、抑制CTL颗粒酶和穿孔素形成 3、降低IFN-γ,IL-2,TNF-α等炎性细胞因子分泌,促进IL-10等免疫抑制因子分泌 4、使T细胞周期停滞在G0/G1期 5、促进肿瘤细胞表皮化,肿瘤转移与浸润
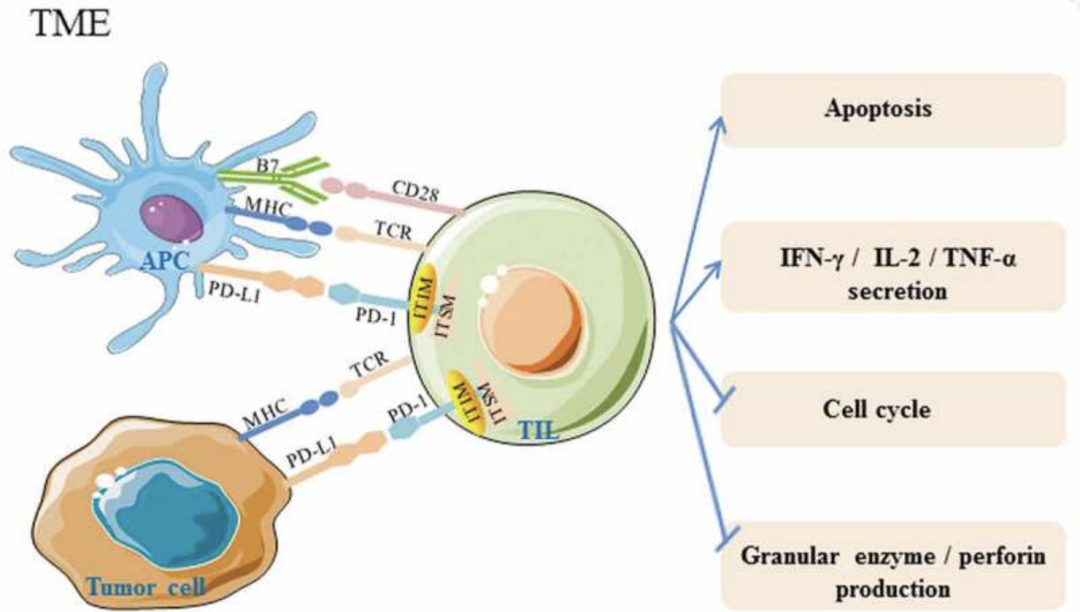
来源:《PD-1 and PD-L1 in cancer immunotherapy: clinical implications and future considerations》 ▉ 下期预告 本期推送中,我们为大家介绍了免疫恢复过程中,机体“稳住T”的策略,即初始T细胞被CTLA-4“困扰”,活化T细胞受PD-1“控制”。
下期推送中,我们将继续介绍免疫恢复过程中其他参与的免疫细胞的去向,敬请期待。 如涉及知识产权请与我司联系
|