▉ 前言 上一期推送中我们为大家介绍了免疫恢复过程中,机体“稳住T”的策略,即初始T细胞被CTLA-4“困扰”,活化T细胞受PD-1“控制”。那么,免疫恢复过程中,免疫细胞又经历了什么?下面就让我们带着好奇,一起来学习一下吧! 
图源:http://werone.co/eng/immunotherapy-non-toxically-with-plants 在开始学习之前,我想先提一个问题:为什么疫苗制造企业要不断研发新疫苗?大家的回答可能是:疫苗企业要靠新产品获得效益;疫苗产品要跟上市场发展,预防新的疾病;……。以上答案都正确。 回到我们的机体,道理也是一样。人体空间是有限的,细胞、抗体是有体积,真实存在的。如果当病原清除后,机体免疫状态依然活跃,这样就免疫过度了,机体内充斥着“过时”的抗体、免疫细胞,一来对新发感染无益,二来也是资源浪费。因此机体需要腾出空间、腾出资源做更有意义的事(随时做好准备应对新发感染)。
那么,机体是如何做的呢?首先,游戏开始前,机体就给不同的免疫细胞和抗体设定了“生命时长”。
中性粒细胞从血液游走后,几天会发生程序性死亡。NK细胞半衰期为一周。如果病原持续存在,中性粒细胞和NK细胞会通过“援军”补充,如果病原去除,它们就会因缺乏补给而慢慢从战场上消失。NK细胞分泌IFN-γ,为巨噬细胞加大“火力”。NK细胞消失,巨噬细胞回到静息状态。DC到达淋巴结后,仅存活一周。浆细胞会在大马力工作五天后力竭而亡。浆细胞产生的抗体,寿命也很短暂,最长的IgG半衰期也不过三周。因此,病原就好比组织中心,病原存在,众兄弟相聚,场面越来越壮观;病原离场,大家散伙,各自西去。 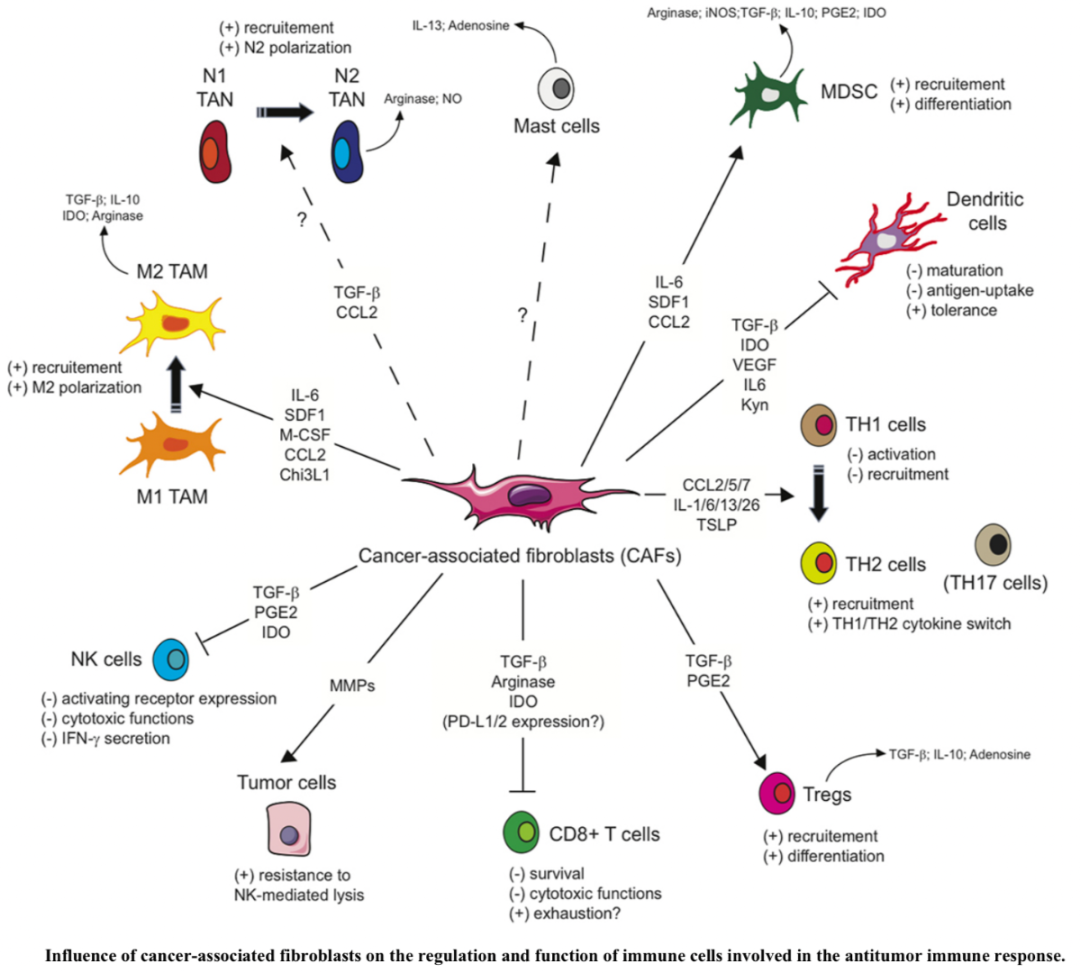
与中性粒细胞、NK细胞不同,T细胞是被寄予厚望的,如果一定要给它的寿命加一个期限,那就是10000年。T细胞是“长寿细胞”,这样设定是有道理的,初始T细胞在二级淋巴器官一遍遍游走,目的就是为寻找展示在表面的抗原。如果T细胞短命,它将很难完成如此重要的使命。 另一方面,当T细胞出色的完成任务后,如果还活力四射,也会给机体带来拥堵(一次杀灭病毒任务,会调动超过10%T细胞。病毒消灭后,如果不清除这些T细胞,会使机体内充斥着如此大量的过时T细胞,造成拥堵)。机体通过AICD(活化诱导的细胞死亡)解决T细胞的问题。AICD机理如下:
CTLs细胞表面含有Fas L蛋白,Fas L可以与靶细胞表面Fas结合,引发CTLs凋亡。未活化T细胞也含有Fas L蛋白,但其是被缠绕状态,因此不会与Fas发生作用。当T细胞活化后,在战场上多次“拼杀”的同时,这种缠绕改变了,其表面Fas L便与Fas作用。因此耗竭T细胞通过Fas介导的杀伤退下战场。通过这种方式,大约90%的T细胞退出战斗舞台。 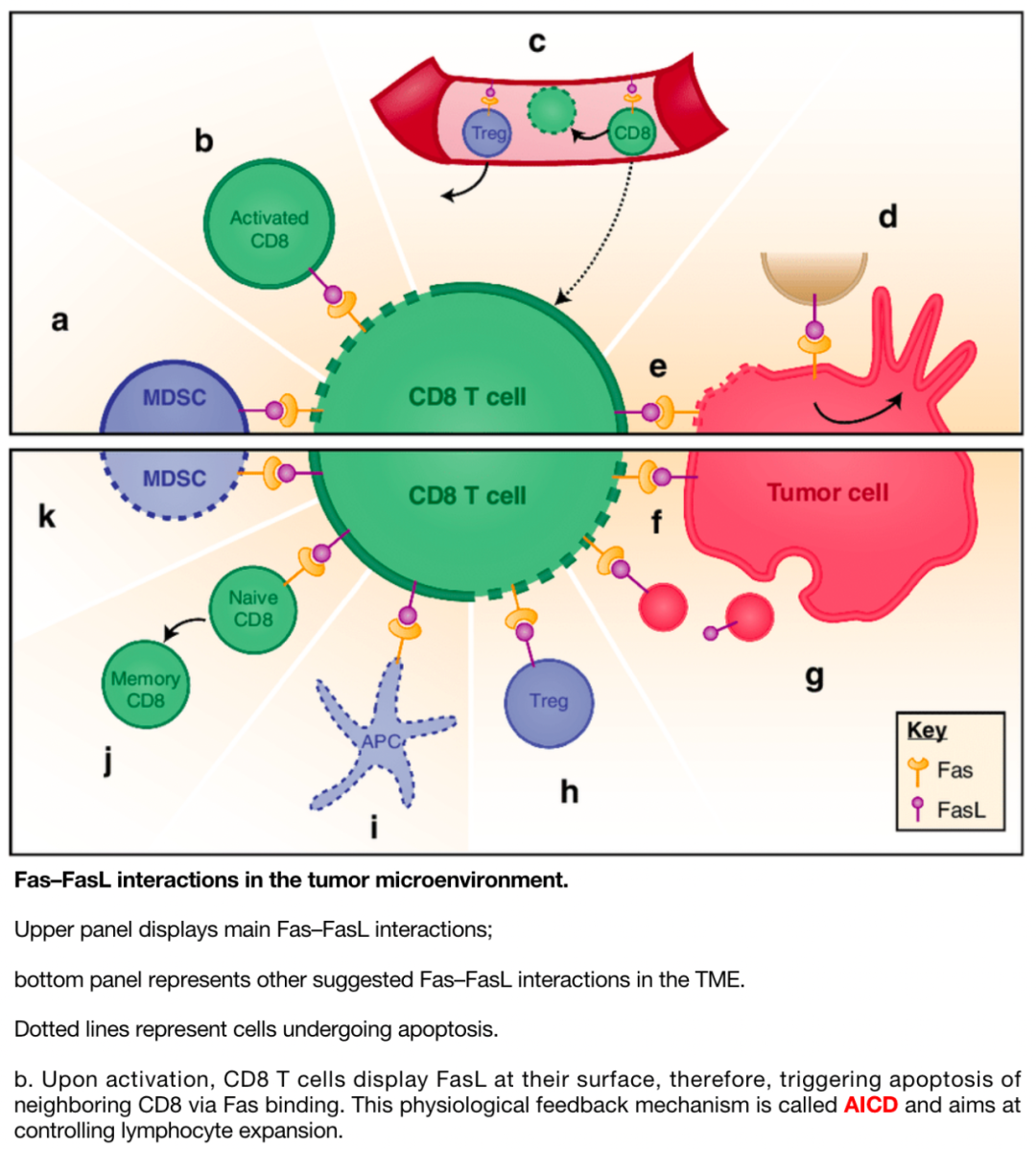 《Apoptosis of tumor-infiltrating T lymphocytes: a new immune checkpoint mechanism》 《Apoptosis of tumor-infiltrating T lymphocytes: a new immune checkpoint mechanism》
▉ 下期预告 本期推送中,我们为大家介绍了免疫恢复过程中中性粒细胞、NK细胞、B细胞及T细胞的结局。下期推送中,我们将开启新的章节,为大家呈现自身耐受和MHC限制的相关知识,敬请期待。 如涉及知识产权请与我司联系
|