来源:生物制品圈
抗体药物包括单克隆抗体药物,抗肿瘤单抗偶联物,双特异性抗体,抗体片段等等。这些药物的靶点主要是细胞表面与疾病相关的抗原或特定的受体分子。抗体进入人体之后,首先与相应抗原发生特异性结合,再通过一系列的生物学作用,如偶联放射性核素的杀伤作用、阻断细胞因子的信号转导、引起补体的级联激活等,进而发挥抗体的治疗作用。
在抗体药物的临床前研发中,一旦确定抗体药物的分子形式并在哺乳动物细胞中表达出抗体蛋白分子后,就需要对抗体的活性进行验证与测定。活性测定是对药物的有效成分和含量以及药物效价的测定,是确保抗体类药物有效性的重要质控指标。目前研发生产中主要通过测定抗体的抗原结合能力来评价活性,常用的方法有ELISA法;流式细胞仪法;一些新技术测定法如SPR技术,目前应用较为广泛的是GE医疗生命科学的Biacore。另外还可以模拟抗体的作用机制,测定其体外生物学活性并进行评价。
一、抗原结合能力测定
1. ELISA法
用ELISA法测定抗体的抗原结合能力一般需要具备相应的可溶性抗原。将可溶性抗原包被于96孔板中,待测抗体与标准品作系列稀释,并分别与酶标抗体混合后加入96孔板,待测抗体与标准品将与酶标抗体竞争结合包被抗原,孵育一段时间后洗脱未结合的抗体,随着待测抗体浓度的降低,酶标抗体与包被抗原的结合量逐渐增加,检测的吸收值逐渐增高,并与待测抗体的浓度呈负相关性。对待测抗体浓度、吸光值作四参数拟合,可得到反“S”形曲线,以曲线的IC50 值评价抗体的抗原结合能力。ELISA方法操作比较简单、耐用性好,为避免标记抗体活性或其他试验因素对测定结果的影响,必须有标准品进行平行操作。
2. 流式细胞仪法
流式细胞仪测定与ELISA法测定原理基本相同,不同的是将可溶性抗原变为细胞,并通过流式细胞仪测定细胞的阳性率指标来检测待测抗体与标记抗体的竞争结合情况。该方法的优点是选用携带抗原的细胞进行检测,细胞表面的抗原空间结构更接近体内存在形式,使待测结果更接近实际情况,另外该方法还避免了相应抗原的制备纯化过程,对于不易获得可溶性抗原的抗体可采用该方法进行测定(图1)。
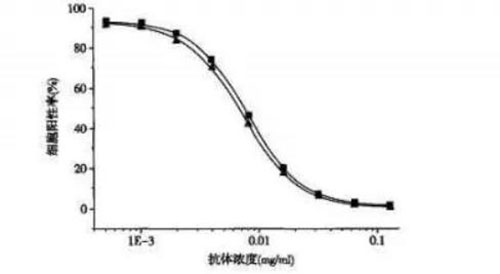
图1 流式细胞仪测定抗体的抗原结合能力
3. 新技术测定法
基于新技术的生物学活性测定方法主要有表面等离子共振效价测定法(SPR)、均相时间分辨荧光、 Alpha 技术、荧光染料标记法等,这里我们主要介绍一下SPR法在蛋白活性测定过程中的应用。
表面等离子共振技术(Surface Plasmon Resonance,SPR)是一种用于生物分子间相互作用分析的新技术,已经成为抗体领域分子互作的“金标准”并被FDA收录。
目前在基础科研和制药行业被广泛应用的仪器是GE医疗生命科学的Biacore。它可以应用于抗体候选物的筛选与评价;抗体与抗原结合活性的分析;抗体与受体结合活性的分析;抗体活性浓度分析;安全性评价中的免疫原性分析;生物类似药一致性分析以及抗体生产质控与批次放行等。
SPR具体测定过程如下:将抗体固定于芯片表面,待测抗原通过微流控系统流经其上,抗原抗体一旦结合,芯片表面的物质质量浓度就会增加,进而引起芯片表面液体折射率的变化而被检测到。该技术测定抗原抗体结合活性时不需要标记,避免了标记对分子结构的影响,能更加真实地反映抗原抗体的结合情况。它测定周期短,样品用量少,一般仅有微克级,可用于微量样品的测定。同时使用亲和力信息及动力学信息来阐述分子间结合机理(图2)。

图2 SPR技术作用原理
1) 抗体与抗原结合活性的分析,抗体候选物的筛选与评价
GE医疗生命科学的Easy Biacore是基于SPR技术,利用捕获法检测抗原抗体之间的相互作用。它主要利用捕获分子与配体之间高亲和的特性,从而实现对配体定向捕获(图3)。该方法操作简便,检测速度快;杂交瘤细胞上清等粗样品可直接上样,无需纯化;芯片可再生后反复使用、运行成本低。罗氏诊断对诊断抗体的筛选也是利用了Biacore的“捕获法”:兔子腹水直接上样,一次性完成130个单抗的筛选,并结合Biacore强大的功能做Ranking得到了最好的Top5目的抗体。

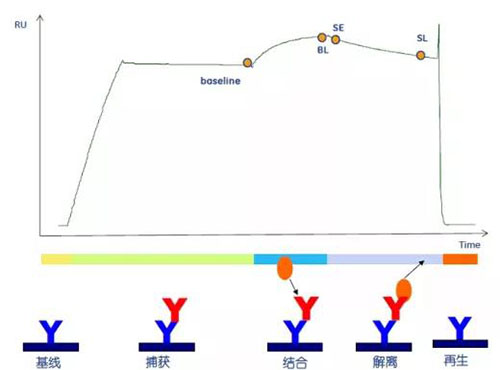
图3 Biacore捕获法检测抗原抗体之间相互作用
2) 抗体与受体结合活性的分析,如抗体与FcγRllla、FcγRlllb 等受体结合的亲和力、动力学信息
2019 年 2 月, 首个国产生物类似药汉利康正式获批上市, 开启了中国生物类似药新时代。在生物类似药的分析相似性评价中,关键一环就是说明药物的结合活性与原研药相似度,从而确定me too or me better。复宏汉霖汉利康®(HLX01)的抗体免疫特性的检测,是基于GE生命科学的 Biacore 完成的。
在抗体-FcγR 受体结合活性分析中,使用 Biacore T200 分别检测了不同抗体与FcγRIa,FcγRIIa,FcγRIIb/c,FcγRIIIa-F,FcγRIIIa-V ,FcγRIIIb 和 FcRn 的结合。Fc 受体结合分析测试的结果显示,HLX01 与 CN-Rituximab 和 EU-Rituxima 结果高度相似(图4)。
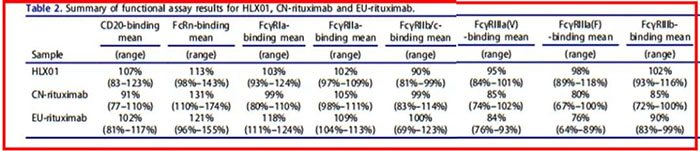

图4 HLX01 与 CN-Rituximab 和 EU-Rituxima 相似性结果
3) 抗体活性浓度分析, 包括基于标准品的活性成分浓度分析和无需依赖标准品的活性成分浓度分析方法
目前,GE医疗生命科学的Biacore基于SPR的无标曲检测法(CFCA calibration-free concentration analysis)可用于蛋白样品的有效活性浓度检测,这种方法直接检测有效互作的分子,无需进行复杂的样品处理和方法建立。结果可靠,简单和精准,或可成为活性蛋白浓度检测基准方法。
Biacore检测是将配体固定在芯片表面,分析物流经芯片表面。在这个过程中,分析物的浓度受到物质迁移速率的影响。CFCA检测可通过分析物以两种流速流经芯片表面,通过物质迁移速率的计算,仪器自动拟合出分析物的浓度(图5)。

图5 分析物在流路管路中由溶液向芯片表面垂直扩散
二、生物学活性测定
1. 补体依赖细胞毒(complement-dependent cytotoxicity,CDC)作用
有些抗肿瘤抗体的作用途径之一是通过补体依赖的细胞毒作用。CDC作用机制如下:抗体先与细胞表面抗原结合形成抗原-抗体复合物,抗体Fc 片段的补体结合位点暴露并与补体C1结合,进而通过后续的补体级联激活途径完成攻膜复合物的装,在细胞表面打孔,最终导致溶细胞效应。
体外测定抗体CDC 作用的过程基本是模拟其体内作用方式。选择具有相应抗原的细胞铺板,加入不同稀释度的抗体孵育,使抗体与细胞表面抗原充分結合,然后再加入补体孵育,结合于细胞表面的抗体将补体成分激活,进而将细胞杀死。由于抗体浓度不同,细胞的杀伤率也不同,对体浓度及吸光度进行四参数曲线拟合可得到反S 形曲线,以其EC 值作为评价抗体CDC 活性的指标。
2. 杀伤活性中和试验
有些细胞因子与其受体结合后能产生细胞杀伤活性,针对该细胞因子的抗体能阻断其与受体的结合,对其杀伤活性其有中和效应。例如,肿瘤坏死因子-α(TNF-α)能与胞表面受体结合并对细胞产生毒性作用。因此人们研制出针对TNF-α的抗体用于类风湿关节炎的治疗。该抗体即可通过杀伤活性中和试验来评价。选择一种对杀伤作用敏感的细胞株, 培养至合适密度后加入96 孔板;用一定浓度TNF-α 溶液将待测抗体及标准品作梯度稀释,然后将各稀释度的抗体溶液加入含有细胞的孔板中孵育, 抗体与TNF-α结合后断了其与细胞表面受体的结合· 中和了其细杀伤活性,因此抗体浓度越高,中和作用越强,细胞的生存率也越高;对活细染色后定OD值,对抗体浓度进行四参数拟合,以EC50值作为评价抗体活性的指标。
3. 细胞增殖抑制试验
增殖抑制试验的原理与杀伤抑制试验相似,同样是通过阻断细胞因子对细胞的作用来反映抗体的活性。该方法中细胞的生长对细胞因子具有依赖作用,当细胞因子与待测抗体结合后, 无法与细胞表面受体结合,细胞在得不到增殖刺激的情况下死亡。抗体浓度越高,增殖抑制作用越强,细胞死亡率越高,继而拟合得到相应的四参数曲线。
4. 荧光素酶报告基因法测定中和活性
由于有些细胞因子与细胞表面受体结合后的信号传导通路已经比较了解,可以在细胞中插入荧光素酶报告基因,如果细胞因子与其受体结合,将引起荧光素酶的表达,通过加入底物显色可以对结合情况进行评价。针对这些细胞因子的单抗可通过荧光素酶报告基因法定中和活性,如针对IL-1β 的卡那奴单抗(canakinumab),测定原理如下:将带有荧光素酶报告基因的铺板,加入梯度稀释的待测单抗及参比品,再加入IL-1β,IL-1β能刺激细胞引起荧光素酶的表达,但抗体与IL-1β 结合能中和其作用。随着抗体浓度的增加, 荧光素酶表达量减少, 两者呈负相关性, 最后加入底物显色并检测,通过平行线分析法计算待测单抗的活性。
分子生物学的快速发展和细胞信号通路的深入研究促进了基于细胞的生物活性测定方法的发展。越来越多的新型技术用于单抗药物的活性检测,可以实现对抗体药物进行精准、多方位、动态的分析,为抗体药物的质量提供了新的保障。
如涉及知识产权请与我司联系
参考文献:
[1]王兰,徐刚领,高凯,王军志. 抗体类生物治疗药物活性测定方法[J].中国生物工程杂志,2015(6):101-108
[2] Patrick E,Anne V H,Michel V,et a1.Surface plasmon resonance:principles, methods and applications in biomedical sciences.Spectroscopy,2003,17(2):255-273.
[3] Guo x.Surface plasmon resonance based biosensor technique:a review.J Biophotonics,2012,5(7):483-501.
|